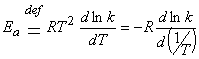La definició de l'energia d'activació aparent
Concepte de l'energia d'activació (activationenergy) va ser per primera vegada per l'equació d'Arrhenius k = Ae-Ea/RT EA proposen els paràmetres. Així es diu l'energia d'activació d'Arrhenius.
El rendiment d'energia d'activació aparent
L'energia d'activació aparent, ja que és a través de les dades experimentals, va cridar els experiments d'energia d'activació. Arrhenius energia d'activació Ea que, estrictament parlant, una funció de la temperatura. Tenint en compte la influència de la temperatura sobre l'Ea, que es va definir com sent igual a LNK-1 / T es multiplica per un pendent negatiu de la corba R.L'energia d'activació aparent per a la reacció química
L'energia d'activació aparent per les reaccions elementals, Ea pot donar significat físic més definit, que significa que l'energia mitjana de l'activació de la biologia molecular i la diferència entre l'energia mitjana de totes les molècules.
L'energia d'activació aparent per les reaccions complexes
L'energia d'activació aparent de reaccions complexes que, si hi ha una clara progressió en l'equació general de la velocitat de reacció, la taxa total constant (també coneguda com l'aparent constant de velocitat) és la constant de velocitat de passos elementals seguit parcel causa de, per exemple:, la reacció total L'energia d'activació és l'energia d'activació de cada àlgebra elemental i, a saber: a = E1 1 / 2E2 I-1 es diu el paquet total quan Ea l'energia d'activació aparent (apparentactivationenergy).
|